 Fulereny 2007-11-10
Fulereny 2007-11-10
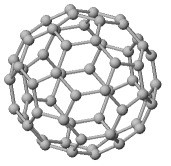 Fulereny to odmiana alotropowa czystego węgla, występującego w formie cząsteczkowej. Należą do nich klastery węglowe Cn o zamkniętej klatkowej budowie pustej w środku.
Fulereny to odmiana alotropowa czystego węgla, występującego w formie cząsteczkowej. Należą do nich klastery węglowe Cn o zamkniętej klatkowej budowie pustej w środku.Najbardziej popularny jest fuleren C60, któremu przypisuje się strukturę klatkową zbudowaną z 12 pierścieni pentagonalnych i 20 pierścieni heksagonalnych. Ilość pierścieni heksagonalnych zgodna jest z twierdzeniem Eulera o izolacji pięciokątów i sprzężonych z nimi sześciokątów dla struktur zamkniętych: m = (n – 20) : 2, gdzie:
m - ilość sześciokątów,
n - ilość równocennych atomów węgla
Fuleren C60 stanowi bryłę 32 – ścienną, której model przedstawiono na rysunku (Zródło: Sussex Fullerene Research Centre, http://www.sussex.ac.uk/Users/kroto/FullereneCentre/gallery/main.html, grudzień 2006). C60 to najbardziej typowy przedstawiciel fulerenów i obok C70 powstaje go najwięcej podczas osadzania się sadzy fulerenowej. Dowodem na to są widma masowe, przedstawione już w pierwszym, przełomowym artykule z 1985 roku autorstwa Sir Harolda Waltera Kroto i jego współpracowników, na którym piki dla C60 i C70 odznaczają się największa intensywnością.
Dla fulerenów, których liczba atomów węgla jest jedną z tzw. liczb magicznych, struktura okazuje się być wyjątkowo trwała. Liczby te to: 60, 70, 72, 76, 78, 84. Zgodnie z przewidywaniami teoretycznymi znaczną trwałością powinny się wyróżniać także fulereny: C140, C180, C240, C260, C420, C540, C560, C960.
Teoretycznie najmniejszym fulerenem może być cząsteczka C20, zbudowana wyłącznie z 12 pierścieni pentagonalnych. Ponieważ w widmach masowych raczej nie obserwuje się piku od klasteru C20, uważa się, że struktura ta jest nietrwała. Zgodnie z obliczeniami teoretycznymi okazało się, że izomery fulerenowe mogą tworzyć cząsteczki C20, C24, C28, C32, C36, C40, C50, z których C32 jest najbardziej stabilnym fulerenem dla n < 60.
Historia odkrycia fulerenów
Do roku 1985 cząsteczka C60 pojawiała się tylko w rozważaniach teoretycznych. Mimo, iż widma masowe klasteru były rejestrowane wcześniej, zainteresowanie naukowców cząstkami Cn o n < 10, odwróciło uwagę od tych unikatowych struktur. Odkrycie fulerenów przypisuje się wspomnianemu Sir Kroto, a doszło do niego przypadkowo. Warto nadmienić, że prof. Kroto, laureat Nagrody Nobla ma „polskie korzenie” – jego dziadkowie pochodzili z Bojanowa, położonego w Wielkopolsce, niedaleko Krotoszyna.
Kroto przy współpracy z Smalleyem i Curlem, przeprowadził serię eksperymentów nad syntezą klasterów węgla, powstających na etapie kondensacji par węglowych, wytworzonych poprzez laserową sublimację grafitu. Widma masowe produktu wskazywały na obecność cząsteczki C60, a intensywność odpowiadającego jej piku zależała od warunków syntezy. Zagadką była struktura molekuły. Dopiero wielogodzinne dyskusje Kroto ze Smalleyem oraz skojarzenie kształtu z kopułami architektonicznymi inżyniera Fullera, doprowadziły do zaproponowania 32 – ściennego modelu, ostatecznie potwierdzonego w późniejszych latach w analizie 13C NMR. Ze względu na skojarzenie kształtu z piłką futbolową, stosowanymi przejściowo nazwami cząsteczki były futbolen i sokeren, ale ostatecznie pozostano przy fulerenie, ku pamięci ekscentrycznego inżyniera. Jednocześnie nazwa ta jest stosowana dla całej rodziny cząsteczek Cn, jako kolejnej odmiany alotropowej węgla.
Właściwości fulerenów
Z punktu widzenia termodynamiki, C60 jest mniej stabilny niż grafit i diament. Fulereny nie rozpuszczają się zbyt dobrze w typowych rozpuszczalnikach organicznych. Do wydobycia ich z sadzy fulerenowej metodą ekstrakcji stosuje się przede wszystkim benzen i toluen, z którymi C60 i C70 dają czerwone i fioletowe roztwory.
Modyfikacja chemiczna fulerenów zmierza w kierunku egzohedralnych, endohedralnych i heterofulerenów. Można je łączyć ze sobą, dzięki czemu otrzymuje się układy o bardzo rozwiniętej powierzchni, dające możliwość wykorzystania ich jako katalizatorów. Te oryginalne cząsteczki mogą znaleźć zastosowanie w inżynierii materiałowej, biofarmaceutyce oraz jako nadprzewodniki. Ciekawostką jest fakt, iż udało się zamknąć we wnętrzu cząsteczki niemalże wszystkie pierwiastki, ale także małe cząsteczki związków chemicznych.
Zródło: N. Łepczyk, Praca magisterska, WCh UW, 2007
Tagi: fulereny C60 C70

 Reklama wspierająca serwis
Reklama wspierająca serwis






